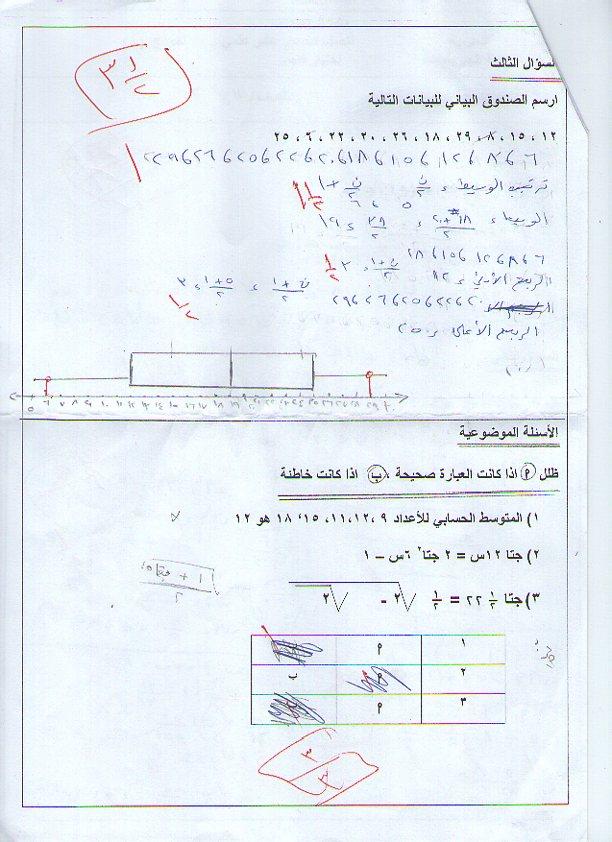
السؤال الثالث :
أكمل الفراغات التالية بما يناسبها :
1 ) عندما تدخل الذرات في التفاعل الكيميائي ، فإنها تعدل من تركيبها الإلكتروني ، في محاولة للوصول إلى حالة
. . . . . . . . . المميز لأقرب . . . . . . . . . لها .
2 ) ترتبط معظم ذرات العناصر مع بعضها البعض عن طريق الروابط . . . . . . . . . أو . . . . . . . . .
3 ) في الرابطة الأيونية . . . . . . . . . ذرة اللافلز إلكترون أو أكثر وتصبح أيون . . . . . . . . . .
4 ) يتحد الصوديوم مع الهيدروجين برابطة . . . . . . . . . لتكوين هيدريد الصوديوم .
5 ) كاتيون الماغنسيوم ( Mg+2 ) يشبه في تركيبه الإلكتروني ذرة غاز. . . . . . . . . .
6 ) تميل فلزات الأقلاء خلال التفاعل الكيميائي . . . . . . . . . إلكترون وتكوين أيون يحمل شحنة . . . . . .
7 ) كاتيون الصوديوم ( Na+ ) . . . . . . . . . استقرارا من ذرة الصوديوم .
8 ) عدد الإلكترونات التي تفقدها ذرة البوتاسيوم عند اتحادها مع الأكسجين تساوي . . . . . . . . . .
9 ) التركيب الإلكتروني لآنيون الكلوريد (Cl- ) والتركيب الإلكتروني لكاتيون البوتاسيوم (K+ ) يشبهان التركيب
الإلكتروني لذرة . . . . . . . . . .
10 ) عدد الإلكترونات الموجودة حول نواة أيون المغنيسيوم (+Mg2 ) يساوي . . . . . . . . . إلكترونات .
11 ) تذوب المركبات الأيونية في المذيبات . . . . . . . . . ولا تذوب في المذيبات . . . . . . . . . .
12 ) عند مرور التيار الكهربائي في مصهور كلوريد الصوديوم ، فإن كاتيونات الصوديوم تتجه نحو القطب الذي يحمل
شحنة . . . . . . . . ، والذي يسمى قطب . . . . . . . . ، بينما تتجه أنيونات الكلوريد نحو قطب . . . . . . . .
13 ) تحدث الرابطة التساهمية بين عناصر بينهم فرق . . . . . . . . . . في السالبية الكهربية .
14 ) التركيب الإلكتروني لذرة الهيدروجين في جزئ الهيدروجين يشبه التركيب الإلكتروني لذرة . . . . . . . .
15 ) تسمى الرابطة التساهمية التي تتكون من زوج واحد من الإلكترونات بالرابطة . . . . . . . . .
16 ) الرابطة التساهمية عبارة عن رابطة . . . . . . . . . . تحدث بين ذرات . . . . . . . . أو . . . . . . . . .
17 ) يوجد بينها فرق . . . . . . . . . في سالبيتها الكهربائية .
18 ) أغلب المركبات . . . . . . . . . لا تذوب في الماء ولكنها تذوب في المذيبات العضوية.
19 ) المركبات التساهمية القطبية تذوب في المذيبات . . . . . . . . .
20 ) قوى التجاذب الكهروستاتيكي بين ذرة الهيدروجين في جزيء ماء وذرة الأكسجين في جزيء ماء مجاور
تسمى رابطة . . . . . . . . . .
21 ) درجة غليان الماء مرتفعة بسبب . . . . . . . . .
22 ) الرابطة بين جزيئات الماء والتي تعمل على شذوذ خواص الماء نتيجة لتجمع جزيئاته تسمى رابطة . . . . . . . .
23 ) الرابطة بين ذرات عنصر الحديد تسمى رابطة . . . . . . . . .
24 ) تزيد قوة الرابطة الفلزية بازدياد عدد . . . . . . . . . و. . . . . . . . . الأيون .
25 ) الفلزات توصل التيار الكهربائي عن طريق حركة . . . . . . . . . خلالها .
السؤال الرابع :
ضع علامة ( ü ) أو علامة ( X) أمام كل عبارة من العبارات التالية :
أكمل الفراغات التالية بما يناسبها :
1 ) عندما تدخل الذرات في التفاعل الكيميائي ، فإنها تعدل من تركيبها الإلكتروني ، في محاولة للوصول إلى حالة
. . . . . . . . . المميز لأقرب . . . . . . . . . لها .
2 ) ترتبط معظم ذرات العناصر مع بعضها البعض عن طريق الروابط . . . . . . . . . أو . . . . . . . . .
3 ) في الرابطة الأيونية . . . . . . . . . ذرة اللافلز إلكترون أو أكثر وتصبح أيون . . . . . . . . . .
4 ) يتحد الصوديوم مع الهيدروجين برابطة . . . . . . . . . لتكوين هيدريد الصوديوم .
5 ) كاتيون الماغنسيوم ( Mg+2 ) يشبه في تركيبه الإلكتروني ذرة غاز. . . . . . . . . .
6 ) تميل فلزات الأقلاء خلال التفاعل الكيميائي . . . . . . . . . إلكترون وتكوين أيون يحمل شحنة . . . . . .
7 ) كاتيون الصوديوم ( Na+ ) . . . . . . . . . استقرارا من ذرة الصوديوم .
8 ) عدد الإلكترونات التي تفقدها ذرة البوتاسيوم عند اتحادها مع الأكسجين تساوي . . . . . . . . . .
9 ) التركيب الإلكتروني لآنيون الكلوريد (Cl- ) والتركيب الإلكتروني لكاتيون البوتاسيوم (K+ ) يشبهان التركيب
الإلكتروني لذرة . . . . . . . . . .
10 ) عدد الإلكترونات الموجودة حول نواة أيون المغنيسيوم (+Mg2 ) يساوي . . . . . . . . . إلكترونات .
11 ) تذوب المركبات الأيونية في المذيبات . . . . . . . . . ولا تذوب في المذيبات . . . . . . . . . .
12 ) عند مرور التيار الكهربائي في مصهور كلوريد الصوديوم ، فإن كاتيونات الصوديوم تتجه نحو القطب الذي يحمل
شحنة . . . . . . . . ، والذي يسمى قطب . . . . . . . . ، بينما تتجه أنيونات الكلوريد نحو قطب . . . . . . . .
13 ) تحدث الرابطة التساهمية بين عناصر بينهم فرق . . . . . . . . . . في السالبية الكهربية .
14 ) التركيب الإلكتروني لذرة الهيدروجين في جزئ الهيدروجين يشبه التركيب الإلكتروني لذرة . . . . . . . .
15 ) تسمى الرابطة التساهمية التي تتكون من زوج واحد من الإلكترونات بالرابطة . . . . . . . . .
16 ) الرابطة التساهمية عبارة عن رابطة . . . . . . . . . . تحدث بين ذرات . . . . . . . . أو . . . . . . . . .
17 ) يوجد بينها فرق . . . . . . . . . في سالبيتها الكهربائية .
18 ) أغلب المركبات . . . . . . . . . لا تذوب في الماء ولكنها تذوب في المذيبات العضوية.
19 ) المركبات التساهمية القطبية تذوب في المذيبات . . . . . . . . .
20 ) قوى التجاذب الكهروستاتيكي بين ذرة الهيدروجين في جزيء ماء وذرة الأكسجين في جزيء ماء مجاور
تسمى رابطة . . . . . . . . . .
21 ) درجة غليان الماء مرتفعة بسبب . . . . . . . . .
22 ) الرابطة بين جزيئات الماء والتي تعمل على شذوذ خواص الماء نتيجة لتجمع جزيئاته تسمى رابطة . . . . . . . .
23 ) الرابطة بين ذرات عنصر الحديد تسمى رابطة . . . . . . . . .
24 ) تزيد قوة الرابطة الفلزية بازدياد عدد . . . . . . . . . و. . . . . . . . . الأيون .
25 ) الفلزات توصل التيار الكهربائي عن طريق حركة . . . . . . . . . خلالها .
السؤال الرابع :
ضع علامة ( ü ) أو علامة ( X) أمام كل عبارة من العبارات التالية :
1 ) عندما تدخل الذرات في التفاعل الكيميائي ، فإنها تعدل من تركيبها الإلكتروني في محاولة للوصول إلى
حالة الاستقرار مثل أقرب غاز نبيل لها .
( )
2 ) التركيب الإلكتروني لآنيون الكبريتيد ( S2- ) يشبه التركيب الإلكتروني لذرة النيون .
( )
3 ) عند إتحاد الصوديوم مع الأكسجين فإن كل ذرة صوديوم تكتسب إلكترون واحد بينما كل ذرة أكسجين تفقد إلكترونين .
( )
حالة الاستقرار مثل أقرب غاز نبيل لها .
( )
2 ) التركيب الإلكتروني لآنيون الكبريتيد ( S2- ) يشبه التركيب الإلكتروني لذرة النيون .
( )
3 ) عند إتحاد الصوديوم مع الأكسجين فإن كل ذرة صوديوم تكتسب إلكترون واحد بينما كل ذرة أكسجين تفقد إلكترونين .
( )